Pada saat aki digunakan, tiap molekul asam sulfat (H2S04) pecah menjadi dua ion hidrogen yang bermuatan positif (2H+) dan ion sulfat yang bermuatan negatif (S04-). Tiap ion S04 yang berada dekat lempeng Pb akan bersatu dengan satu atom timbal murni (Pb) menjadi timbal sulfat (PbS04) sambil melepaskan dua elektron. Sedang sepasang ion hidrogen tadi akan ditarik lempeng timbal dioksida (PbO2), mengambil dua elektron dan bersatu dengan satu atom oksigen membentuk molekul air (H2O).
Dari proses ini terjadi pengambilan elektron dari timbal dioksida (sehingga menjadi positif) dan memberikan elektron itu pada timbal murni (sehingga menjadi negatif), yang mengakibatkan adanya beda potensial listrik di antara dua kutub tersebut. Proses tersebut terjadi secara simultan, reaksi secara kimia dinyatakan sebagai berikut :
Pb02 + Pb + 2H2S04 —–> 2PbS04 + 2H20
Di atas ditunjukkan terbentuknya timbal sulfat selama penggunaan (discharging). Keadaan ini akan mengurangi reaktivitas dari cairan elektrolit karena asamnya menjadi lemah (encer), sehingga tahanan antara kutub sangat lemah untuk pemakaian praktis.
Sementara proses kimia selama pengisian aki (charging) terjadi setelah aki melemah (tidak dapat memasok arus listrik pada saat kendaraan hendak dihidupkan). Kondisi aki dapat dikembalikan pada keadaan semula dengan memberikan arus listrik yang arahnya berlawanan dengan arus yang terjadi saat discharging. Pada proses ini, tiap molekul air terurai dan tiap pasang ion hidrogen yang dekat dengan lempeng negatif bersatu dengan ion S04 pada lempeng negatif membentuk molekul asam sulfat. Sedangkan ion oksigen yang bebas bersatu dengan tiap atom Pb pada lempeng positif membentuk Pb02. Reaksi kimia yang terjadi adalah :
2PbS04 + 2H20 —-> PbO2 + Pb + 2H2S02
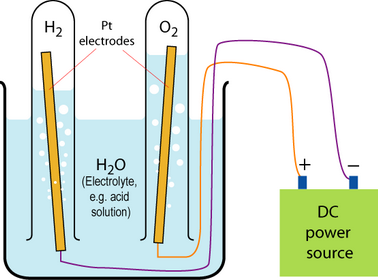
PERUBAHAN KIMIA SELAMA PENGISIAN DAN PEMAKAIAN
Pemakaian
![[Image: pemakaian.gif]](http://www.gs.astra.co.id/ina/library/image/pemakaian.gif)
Pengisian
![[Image: pengisian.gif]](http://www.gs.astra.co.id/ina/library/image/pengisian.gif)
Kondisi Bermuatan Penuh [/b] Kondisi Terpakai Habis
Pelat(+) Elektrolit 2H2SO4 PEMAKAIAN Pelat(+) Elektrolit Pelat(-)
PB02 Timbal + Asam Sulfat dan Air - -----------> PbSO4 Timbal Sulfat + 2H2O air + PbSO4
Peroksida <---------- Timbal
PENGISIAN Sulfat
1. PERUBAHAN KIMIA PADA SAAT PELEPASAN MUATAN LISTRIK
Aki memberikan aliran listrik jika dihubungkan dengan rangkaian luar misalnya, lampu, radio dan lain-lain. Aliran listrik ini terjadi karena reaksi kimia dari asam sulfat dengan kedua material aktif dari plat positif dan plat negatif. Pada saat pelepasan muatan listrik terus menerus, elektrolit akan bertambah encer dan reaksi kimia akan terus berlangsung sampai seluruh bahan aktif pada permukaan plat positif dan negatif berubah menjadi timbal sulfat. Jika Aki tidak dapat lagi memberi aliran listrik pada voltage tertentu, maka aki tersebut dalam keadaan lemah arus (soak).
2. PERUBAHAN KIMIA PADA SAAT PENGISIAN MUATAN LISTRIK
Pada proses pengisian muatan listrik, kembali terjadi proses reaksi kimia yang berlawanan dengan reaksi kimia pada saat pelepasan muatan. Timbal peroksida terbentuk pada plat positif dan timbal berpori terbentuk pada plat negatif, sedangkan berat jenis elektrolit akan naik, karena air digunakan untuk membentuk asam sulfat. Aki kembali dalam kondisi bermuatan penuh.
PENURUNAN BERAT JENIS ACCU ZUUR
SELAMA PELEPASAN MUATAN LISTRIK
Berat jenis accu zuur akan turun sebanding dengan derajat pelepasan muatan, jadi jumlah energi listrik yang ada dapat ditentukan dengan mengukur berat jenis accu zuurnya, misalnya aki mempunyai berat jenis accu zuur 1.260 pada 20°C, bermuatan listrik penuh, setelah melepaskan muatan listrik berat jenisnya 1.200 pada 20°C, maka Aki masih mempunyai energi listrik sebesar 70%
![[Image: beratjenis.gif]](http://www.gs.astra.co.id/ina/library/image/beratjenis.gif)
Pemakaian
![[Image: pemakaian.gif]](http://www.gs.astra.co.id/ina/library/image/pemakaian.gif)
Pengisian
![[Image: pengisian.gif]](http://www.gs.astra.co.id/ina/library/image/pengisian.gif)
Kondisi Bermuatan Penuh [/b] Kondisi Terpakai Habis
Pelat(+) Elektrolit 2H2SO4 PEMAKAIAN Pelat(+) Elektrolit Pelat(-)
PB02 Timbal + Asam Sulfat dan Air - -----------> PbSO4 Timbal Sulfat + 2H2O air + PbSO4
Peroksida <---------- Timbal
PENGISIAN Sulfat
1. PERUBAHAN KIMIA PADA SAAT PELEPASAN MUATAN LISTRIK
Aki memberikan aliran listrik jika dihubungkan dengan rangkaian luar misalnya, lampu, radio dan lain-lain. Aliran listrik ini terjadi karena reaksi kimia dari asam sulfat dengan kedua material aktif dari plat positif dan plat negatif. Pada saat pelepasan muatan listrik terus menerus, elektrolit akan bertambah encer dan reaksi kimia akan terus berlangsung sampai seluruh bahan aktif pada permukaan plat positif dan negatif berubah menjadi timbal sulfat. Jika Aki tidak dapat lagi memberi aliran listrik pada voltage tertentu, maka aki tersebut dalam keadaan lemah arus (soak).
2. PERUBAHAN KIMIA PADA SAAT PENGISIAN MUATAN LISTRIK
Pada proses pengisian muatan listrik, kembali terjadi proses reaksi kimia yang berlawanan dengan reaksi kimia pada saat pelepasan muatan. Timbal peroksida terbentuk pada plat positif dan timbal berpori terbentuk pada plat negatif, sedangkan berat jenis elektrolit akan naik, karena air digunakan untuk membentuk asam sulfat. Aki kembali dalam kondisi bermuatan penuh.
PENURUNAN BERAT JENIS ACCU ZUUR
SELAMA PELEPASAN MUATAN LISTRIK
Berat jenis accu zuur akan turun sebanding dengan derajat pelepasan muatan, jadi jumlah energi listrik yang ada dapat ditentukan dengan mengukur berat jenis accu zuurnya, misalnya aki mempunyai berat jenis accu zuur 1.260 pada 20°C, bermuatan listrik penuh, setelah melepaskan muatan listrik berat jenisnya 1.200 pada 20°C, maka Aki masih mempunyai energi listrik sebesar 70%
![[Image: beratjenis.gif]](http://www.gs.astra.co.id/ina/library/image/beratjenis.gif)

waw,,pinter buuanget,,boleh tanya neng yang mengambil 2 elektron,ion h+ atau lempeng pbo2?
BalasHapus